Vảy nến là bệnh da mạn tính thường gặp với các biểu hiện đặc trưng. Tỷ lệ mắc vảy nến trên bệnh nhân HIV so với dân số bình thường là tương đương nhưng đặc điểm lâm sàng đa dạng, không điển hình và thường kháng điều trị. Lựa chọn phương pháp điều trị trên đối tượng này vẫn còn hạn chế do nguy cơ gây tử vong liên quan đến thuốc ức chế miễn dịch cổ điển và thuốc sinh học mới. Mặc dù, trong những năm gần đây, các liệu pháp điều trị vảy nến bằng thuốc trên bệnh nhân HIV đã có những tiến bộ lớn. Bài viết đề cập đến các biểu hiện lâm sàng hay gặp, sinh bệnh học cũng như những bằng chứng về hiệu quả điều trị những phương pháp điều trị vảy nến trên bệnh nhân HIV.
1. Sinh bệnh học vảy nến ở bệnh nhân HIV
Vảy nến là một bệnh lý viêm mạn tính liên quan đến sự biểu hiện quá mức của các cytokin type 1 (TNF-alpha, IL-12, IL-23). Như vậy, biểu hiện nặng của vảy nến ở bệnh nhân suy giảm miễn dịch như nhiễm HIV giai đoạn tiến triển dường như có sự mâu thuẫn. Dưới đây chúng tôi đề cập đến một số cơ chế sinh lý bệnh giải thích rõ hơn về biểu hiện vảy nến trên bệnh nhân HIV.
1.1 Những thay đổi trong tiểu quần thể tế bào lympho
Trên bệnh nhân HIV có sự giảm số lượng tế bào lympho TCD4+, số lượng tế bào TCD8+ tăng lên dẫn đến sự mất cân bằng giữa tỷ lệ TCD4+/TCD8+, điều này góp phần làm rối loạn cân bằng nội môi hình thành các biểu hiện lâm sàng của vảy nến.
Tăng số lượng tế bào TCD8+ nhớ, giảm số lượng tế bào TCD8+ ngây thơ có liên quan đến cơ chế bệnh sinh vảy nến trên bệnh nhân nhiễm HIV.
Rối loạn chức năng điều hòa của tế bào lympho Foxp3+ có thể liên quan đến sinh bệnh học của bệnh. Tế bào này chịu trách nhiệm ức chế miễn dịch tế bào và tạo ra khả năng dung nạp miễn dịch thông qua con đường miễn dịch tế bào trực tiếp (gây độc tế bào) hoặc thông qua tiết chất trung gian chống viêm như IL-10. Trên bệnh nhân vảy nến, có tăng các tế bào T điều hòa nhưng những tế bào này bị rối loạn chức năng. Mặt khác, ở bệnh nhân HIV, các mô ngoại vị có tăng số lượng tế bào T điều hòa với chức năng được duy trì, ý nghĩa của sự gia tăng này trên bệnh nhân có biểu hiện vảy nến vẫn chưa được rõ ràng.
1.2 Sự thay đổi bài tiết các cytokine
Bệnh nhân HIV có sự chuyển đổi từ các cytokine type 1 sang type 2 dẫn đến tăng cytokine type 2 (IL-4, IL6, IL-10), giảm cytokine type 1 (TNF -alpha, IFNc, IL-2). Điều này giúp giải thích được tình trạng tăng gamma globulin (kích thích bởi cytokine type 2) và giảm khả năng đáp ứng với các vi sinh vật nội bào (thông qua các cytokine type 1) ở bệnh nhân HIV. Tuy nhiên, cơ chế bệnh sinh của vảy nến liên quan với các cytokine type 1 do đó bằng chứng này gây ra sự mâu thuẫn khi tình trạng vảy nến nặng hơn ở bệnh nhân HIV. Các báo cáo đã đưa ra được chứng minh, trên bệnh nhân HIV tăng cytokine type 2 nhưng đồng thời có sự tăng sản xuất cytokine type 1 ở ngoại vi bởi các tế bào TCD8+.
1.3 Sự biểu hiện quá mức của HLA-DR
HLA-DR là kháng nguyên phức hợp hòa hợp mô chủ yếu lớp II, đóng vai trò quan trọng trong trình diện kháng nguyên và hiếm khi được biểu hiện trong lớp thượng bì người khỏe mạnh. Tuy nhiên, thông qua gamma globulin, tế bào sừng có thể biểu lộ HLA-DR. Trong những trường hợp có sự gia tăng giải phóng gamma interferon như trong nhiễm HIV, tế bào sừng có sự biểu hiện quá mức của HLA-DR gây ra quá trình di chuyển bạch cầu vào mô da và làm tăng phản ứng với liên cầu, tụ cầu thúc đẩy hình thành các kiểu hình vảy nến.
1.4 Siêu kháng nguyên
Các siêu kháng nguyên là các phân tử có khả năng gây ra các đáp ứng trực tiếp, không đặc hiệu, đa dòng các tế bào lympho T, giải phóng một lượng lớn cytokine có thể liên quan đến bệnh vảy nến. Các siêu kháng nguyên kết hợp với phức hợp HLA-DR gây ra sự trình diện kháng nguyên và thâm nhập bạch cầu vào mô da góp phần hình thành nên vảy nến mảng. Các siêu kháng nguyên tụ cầu và liên cầu liên quan đến bệnh sinh của vảy nến và các đợt cấp vảy nến trên bệnh nhân nhiễm HIV. Ngoài ra, bệnh nhân HIV có các siêu kháng nguyên là một số protein của virus như protein nef và gp120 góp phần làm nặng vảy nến.
1.5 Bắt chước phân tử
Bắt chước phân tử là khả năng trong đó chuỗi trình tự tương đồng giữa các peptit ngoại lai và peptit tự thân có thể đủ để dẫn đến sự hoạt hóa chéo của các tế bào T hoặc B tự hoạt động khi có mặt protein gây bệnh.
Bắt chước phân tử có thể liên quan đến phản ứng tự miễn dịch do protein HIV gây ra. Trên thực tế, có sự tương đồng về cấu trúc giữa các protein của HIV-1 với các phân tử khác nhau liên quan đến phản ứng miễn dịch, chẳng hạn như HLA-DR4 và DR-2; phần biến đổi của thụ thể TCR alpha, beta và gamma; protein Fas; và một số miền chuỗi nặng IgG và IgA. Do đó, các protein env có thể là một phần của phản ứng miễn dịch khuếch đại tự thân, dẫn đến các phản ứng viêm mãn tính và cuối cùng là tổn thương vảy nến. Tuy nhiên, cơ chế chính xác và ý nghĩa của bắt chước phân tử trong quá trình sinh bệnh học của vảy nến vẫn chưa được hiểu biết đầy đủ.
1.6 Các giả thuyết khác
HIV tác động trực tiếp lên tăng sinh tế bào sừng. Giả thuyết này ủng hộ cho việc trong tế bào langerhans của da có tải lượng virus cao hơn, tương quan trực tiếp đến tình trạng nặng hơn của vảy nến. Các cơ chế chưa được làm rõ nhưng có thể liên quan đến tác dụng protein tat.
Giả thuyết khác cho rằng nhiễm HIV dẫn đến tái hoạt động của các retrovius nội sinh với đáp ứng miễn dịch chống lại chúng.
2. Biểu hiện lâm sàng
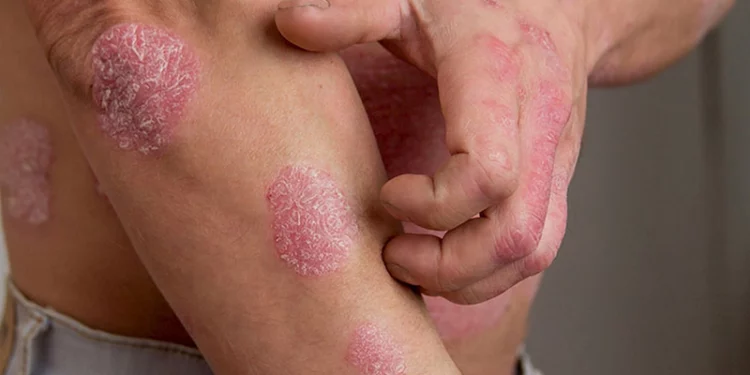
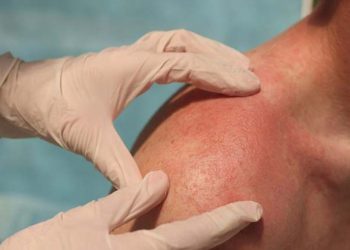
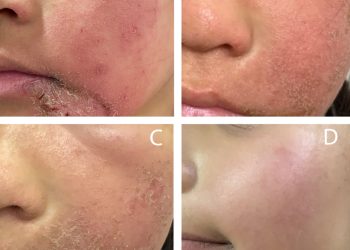
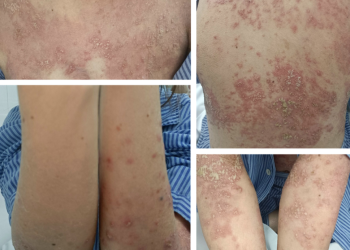
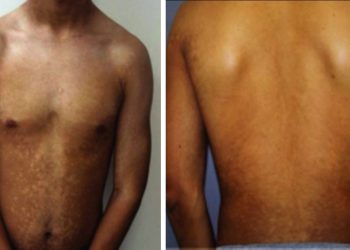
Biểu hiện vảy nến trên bệnh nhân HIV đa dạng và có thể có đồng thời nhiều dạng tổn thương. Trên lâm sàng, có thể nghi ngờ nhiễm HIV khi thay đổi đột ngột tình trạng bệnh hoặc chẩn đoán vảy nến với các biểu hiện không điển hình.
Tại Mỹ, vảy nến thể mảng là thể bệnh thường gặp nhất ở bệnh nhân HIV, tương tự như những trường hợp mắc vảy nến không nhiễm HIV. Tuy nhiên, ở châu Phi hạ Sahara biến thể thường gặp nhất là đỏ da toàn thân vảy nến. Sự khác biệt này có thể do chẩn đoán muộn hoặc suy giảm mức độ nặng vì thiếu liệu pháp kháng virus tích cực (HARRT). Biểu hiện lâm sàng này cần chẩn đoán phân biệt với phát ban do thuốc và u lympho T ở da trên bệnh nhân HIV.
Trên bệnh nhân HIV, tỷ lệ xuất hiện tổn thương dạng vảy nến da dầu (sebopsoriasis) tăng. Đây là hình thái có lâm sàng chồng lấp giữa vảy nến thể mảng và viêm da dầu, hay gặp ở vị trí nếp gấp, da đầu và vùng sau tai, thường có vảy dày và dính. Vảy nến da dầu đáp ứng tốt với thuốc bôi và liệu pháp kháng nấm đường toàn thân.
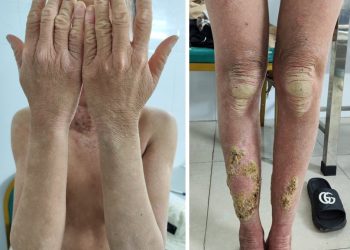
Vảy nến dạng vảy ốc (rupiod psoriasis) là dạng hiếm gặp nhất của vảy nến, có mối liên quan chặt chẽ với nhiễm HIV. Hình thái đặc trưng là sẩn hình nón, hình đồng xu, vảy tiết dày và thường ở phía dưới của thân mình.
Viêm khớp vảy nến thường gặp hơn và tình trạng phá hủy khớp tăng lên
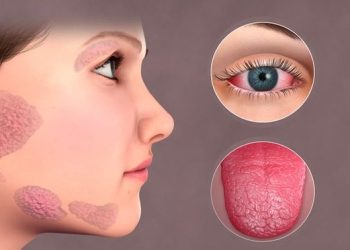
Viêm khớp phản ứng Reiter là một bệnh lý thoái hóa đốt sống có huyết thanh âm tính đặc trưng bởi bộ ba triệu chứng: viêm niệu đạo, viêm khớp và viêm kết mạc. Mối liên quan giữa viêm khớp phản ứng và vảy nến thường xảy ra hơn ở những người nhiễm HIV. Biểu hiện da thường gặp nhất là mảng thâm nhiễm dạng vảy nến vùng lòng bàn tay và bàn chân (keratoderma blennorrhagicum).
Biểu hiện vảy nến trên bệnh nhân HIV cần chẩn đoán phân biệt với giang mai II, viêm da dầu, phát ban do thuốc.
3. Điều trị
Điều trị vảy nến trên bệnh nhân HIV có tình trạng kháng trị và tỷ lệ tái phát cao hơn nhóm người không nhiễm HIV. Ngoài ra, các phương pháp điều trị bằng thuốc ức chế miễn dịch toàn thân và thuốc sinh học gây suy giảm miễn dịch hệ thống nên chỉ định bị giới hạn.
Dưới đây là phương pháp điều trị vảy nến trên bệnh nhân nhiễm HIV.
3.1 Liệu pháp tại chỗ
Điều trị tại chỗ với corticosteroid, dẫn xuất tổng hợp của vitamin D3 là liệu pháp đơn trị liệu đầu tay đối với vảy nến mức độ nhẹ đến trung bình và kết hợp với các phương thức điều trị khác trong vảy nến mức độ nặng. Trong báo cáo về ca bệnh đỏ da toàn thân vảy nến không đáp ứng với etritinate 75mg/ngày nhưng triệu chứng đỏ da đáp ứng hoàn toàn với calcipotriol tại chỗ. Không có báo cáo nào về việc tăng tỷ lệ hoặc mức độ nghiêm trọng khi dùng thuốc trên những đối tượng này.
3.2 Liệu pháp kháng virus tích cực (Highly active antiretroviral therapy – HAART)
HAART là liệu pháp đầu tay ở những bệnh nhân vảy nến mức độ từ trung bình đến nặng, đặc biệt khi có số lượng tế bào CD4+ <350 tế bào / mm3, và trong một số trường hợp có thể xem xét là liệu pháp đơn trị liệu. HAART không chỉ làm thay đổi quá trình tiến triển tự nhiên của nhiễm HIV mà còn kiểm soát hiệu quả vảy nến. Một số báo cáo nghiên cứu về các trường hợp có đáp ứng điều trị đáng kể với HAART. Trong nghiên cứu mở duy nhất được công bố cho đến nay, zidovudine giúp cải thiện lâm sàng ở 90% bệnh nhân vảy nến.
3.3 Liệu pháp ánh sáng
PUVA hoặc NB-UVB được chỉ định trên những bệnh nhân không kiểm soát bằng thuốc bôi tại chỗ và HAART. Liệu pháp ánh sáng ở bệnh nhân HIV có hiệu quả tương tự như những người bệnh vảy nến không có HIV. Một số tác giả cho rằng PUVA nên được ưu tiên hơn NB-UVB vì lợi ích cao hơn nguy cơ. Tuy nhiên, vấn đề này vẫn còn nhiều tranh cãi. Trong hướng dẫn điều trị của Học viện Da liễu Hoa Kỳ không đưa ra khuyến nghị về việc liệu pháp ánh sáng nào nên được ưu tiên như lựa chọn hàng đầu, trong hướng dẫn S3 của Châu Âu khuyến nghị có thể áp dụng NB-UVB là phương pháp điều trị ban đầu thay vì phác đồ PUVA.
Phân tích điều trị gần đây của Quỹ tài trợ vảy nến quốc gia Mỹ đưa ra cân nhắc về tính an toàn nên ưu tiên lựa chọn NB-UVB mặc dù PUVA có hiệu quả lâu dài hơn so.
Liệu pháp ánh sáng chống chỉ định trên bệnh nhân Kaposi’s sarcoma vì ảnh hường xấu đến tiên lượng bệnh.
3.4 Uống retinoid
Với các trường hợp không đáp ứng với điều trị bằng thuốc bôi tại chỗ, HAART và liệu pháp quang trị liệu, retinoid đường uống là khuyến cáo được lựa chọn điều trị. Retinoids đường uống có hiệu quả trong việc kiểm soát bệnh, có tác dụng hiệp đồng với liệu pháp quang trị liệu, do đó cho phép giảm liều lượng bức xạ được sử dụng mà không làm tăng nguy cơ ức chế miễn dịch. Trong hầu hết các trường hợp, liều acitretin tương tự bệnh nhân không nhiễm HIV 0.5–1 mg /kg /ngày. Trong một số trường hợp dai dẳng kháng trị có thể cần phải tăng liều điều trị.
Hiệu quả và tính an toàn của retinoid đường uống giống như ở bệnh nhân không nhiễm HIV. Trong điều trị cần chú ý đến tương tác với một số loại thuốc kháng virus kháng retrovirus vì có thể làm tăng nguy cơ tăng triglycerid máu và viêm tụy.
3.5 Thuốc ức chế miễn dịch đường uống
Bởi vì những rủi ro nghiêm trọng liên quan đến ức chế miễn dịch trên bệnh nhân nhiễm HIV nên thuốc chỉ được chỉ định giới hạn ở những bệnh nhân kháng trị. Bằng chứng điều trị hạn chế, thông qua các trường hợp lâm sàng hoặc một số báo cáo các ca bệnh số lượng nhỏ.
3.5.1 Cyclosporin
Là thuốc ức chế calcineurin. Gần đây, các khuyến cáo điều trị đều đưa ra các cảnh báo thận trọng khi điều trị ngay cả trong trường hợp miễn dịch bình thường. Cyclosporin chỉ định với mục đích gây đáp ứng điều trị nhanh trong các trường hợp nặng, đợt điều trị ngắn hạn và việc sử dụng thuốc lâu dài (tối đa là hai năm) cần lựa chọn bệnh nhân. Mặc dù các báo cáo về hiệu quả điều trị làm thuyên giảm các biểu hiện lâm sàng và không gây suy giảm miễn dịch đáng kể ở các bệnh nhân vảy nến nhiễm HIV, cyclosporin cần lựa chọn chỉ định trên những bệnh nhân đặc biệt như đỏ da toàn thân vảy nến. Cyclosporin luôn phải kết hợp với HAART và cần theo dõi lâm sàng chặt chẽ, nguy cơ tăng huyết áp nặng và khả năng gây độc cho thận. Phác đồ chuẩn là cyclosporin 2–2,5 mg/kg/ngày trong 12–24 tuần.
3.5.2 Methotrexate
Do các báo cáo về biến chứng điều trị vảy nến bằng methotrexate trên bệnh nhân HIV như nhiễm trùng cơ hội, methotrexate bị chống chỉ định trong điều trị khi có nhiễm HIV. Gần đây, với sự ra đời của HAART và các liệu pháp mới, methotrexate được chỉ định điều trị với liều thấp hơn. Khi sử dụng methotrexate, các khuyến cáo hiện tại yêu cầu đánh giá theo từng trường hợp và áp dụng đồng thời HAART cũng như dự phòng nhiễm trùng cơ hội. Nên loại trừ nhiễm HBV trước khi bắt đầu dùng methotrexate, vì thuốc có nguy cơ tái hoạt viêm gan B.
3.6 Thuốc sinh học
3.6.1 Ức chế TNF-alpha
Thuốc ức chế TNF-alpha (adalimumab, infliximab, enternacept) được coi là một mốc trong lịch sử điều trị vảy nến vì đạt hiệu quả cao ngay cả trên các đối tượng thất bại với phương pháp điều trị khác, đặc biệt trên bệnh nhân biểu hiện cả trên da và khớp. Trong các báo cáo, thuốc có nguy cơ suy giảm miễm dịch gây tăng tỉ lệ tử vong do biến chứng nhiễm trùng và không nhiễm trùng. Cần kiểm soát lao chặt chẽ do tỉ lệ tái phát lao đáng kể khi sử dụng thuốc ức chế TNF-alpha. Do vậy, chỉ định điều trị trên bệnh nhân nhiễm HIV cần có sự lựa chọn kĩ, khi bệnh nhân không đáp ứng với liệu pháp khác, tình trạng HIV được kiểm soát và không giảm CD4+. Dựa trên các báo cáo trường hợp lâm sàng, với những bệnh nhân thích hợp thuốc kháng TNF-alpha có thể được coi là một lựa chọn hàng thứ ba, nhưng chỉ định điều trị bằng vẫn còn nhiều hạn chế.
3.6.2 Thuốc kháng IL-12 / IL-23 (Ustekinumab)
Báo cáo lâm sàng về sử dụng ustekinumab ít hơn so với các thuốc kháng TNF-alpha. Tuy nhiên có báo cáo mô tả điều trị thành công vảy nến trên bệnh nhân nhiễm HIV với ustekinumab, bệnh nhân đã đạt được sự cải thiện đáng kể về tình trạng vảy nến và điều trị được dung nạp tốt.
3.6.3 Các thuốc khác
Các báo cáo về khả năng dung nạp của secukinumab, ixekizumab, brodalumab, guselkumab và tildrakizumab trong bệnh nhân nhiễm HIV chưa được đánh giá. Tuy nhiên, với cơ chế hoạt động của những loại thuốc này cho thấy nguy cơ gây trầm trọng bệnh HIV thấp.
3.7 Thuốc kháng phosphodiesterase-4 đường uống (apremilast)
Apremilast là một lựa chọn điều trị cho bệnh nhân nhiễm HIV vì thuốc hầu như không có tác dụng ức chế miễn dịch đáng kể. Điều trị được dung nạp tốt ở bệnh nhân đồng nhiễm HIV và virus viêm gan C (HCV)
4. Kết luận
Nhiễm HIV là một yếu tố nguy cơ độc lập của bệnh vảy nến nặng và trên một số bệnh nhân, vảy nến là dấu hiệu ban đầu của nhiễm HIV với biểu hiện lâm sàng đa dạng, kháng trị và tái phát Điều trị vảy nến trên bệnh nhân nhiễm HIV có nhiều thách thức và tác dụng ức chế miễn dịch của các liệu pháp điều trị bệnh vảy nến là mối quan tâm hàng đầu. Với vảy nến mức độ từ trung bình đến nặng trên bệnh nhân nhiễm HIV thì HAART, retinoids uống và liệu pháp quang trị liệu kết hợp với thuốc bôi vẫn là điều trị chuẩn. Thuốc TNF-alpha được cân nhắc là lựa chọn điều trị thứ 3 nhưng cần lựa chọn bệnh nhân và kiểm soát kĩ khi điều trị. Với tác dụng phụ gây nguy cơ nhiễm trùng cơ hội, methotrexate và cylosporin cần tránh.
Tài liệu tham khảo:
- Treatment selection for moderate to severe plaque psoriasis in special populations, April W Armstrong, MD, MPH, uptodate, Feb 2021.
- Psoriasis in HIV infection: an update, Miguel Alpalhao, J. Borges-Costa and Paulo Filipe, International Journal of STD & AIDS, Jan 2019
- Psoriasis: Which therapy for which patient: Focus on special populations and chronic infections, Shivani B. Kaushik, MD, and Mark G. Lebwohl, MD, The American Academy of Dermatology, Jan 2019
Tác giả: TS.BS. Nguyễn Thị Hà Vinh, BSNT. Nguyễn Thị Huế
Nguồn: Dalieu.vn